28 ноября 2019
Поговорим о нейроэндокринных опухолях?
Вариативность диагностических критериев и терапевтических подходов у пациентов с НЭО
Впервые нейроэндокринная опухоль (НЭО) была описана Отто Лурбаршем еще в 1867 году [1]. Ранее эти опухоли считались крайне редкими, однако за последние 30 лет их распространенность выросла почти в 6 раз [2]. Сегодня ежегодная заболеваемость в Соединенных Штатах составляет приблизительно 3,65 на 100 000 населения [3].
Еще в 1980 году были предприняты первые попытки систематизировать классификацию НЭО [4]. С тех пор выявляемость НЭО существенно возросла, и эксперты ВОЗ регулярно обновляли и дополняли классификацию. Однако эти документы были сложными отчасти потому, что морфологически сходные НЭО были обозначены по-разному в зависимости от места происхождения, что создавало диагностические «серые зоны». К тому же, согласно ряду исследований, низкая дифференцировка препарата опухоли не всегда однозначно говорит о ее высокой степени злокачественности [5-7].
Однако такие особенности, как индекс пролиферации опухоли и степень локального распространения, были общими для большинства версий классификации. В 2010 г. экспертами ВОЗ предложена классификация НЭО, разработанная на базе консенсуса международных экспертов по НЭО и с учетом классификаций Европейского общества по нейроэндокринным опухолям (ENETS), Американского объединенного комитета по онкологии (AJCC) и Североамериканского общества по изучению НЭО (NANETS). Предложенная классификация опирается на следующие характеристики НЭО: наличие молекулярных мутаций, функциональную активность, гистологические особенности и стадию заболевания. В этой классификации года общий термин для всех опухолей нейроэндокринного происхождения – «нейроэндокринная опухоль» (НЭО) – изменен на «нейроэндокринная неоплазия» (НЭН). Согласно этой классификации, выделяют 3 группы НЭН – НЭО G1, НЭО G2 и нейроэндокринная карцинома (НЭК) G3 и смешанную адено-нейроэндокринную карциному.
Самая последняя классификация ВОЗ 2019 года теперь включает новую категорию высокодифференцированных НЭО G3 с индексом пролиферации Ki-67 более 20% (таблица 1). Классификация ВОЗ 2019 совершенствует градацию НЭН ЖКТ И ПЖ и заполняет диагностические «серые зоны» [8].
Таблица 1
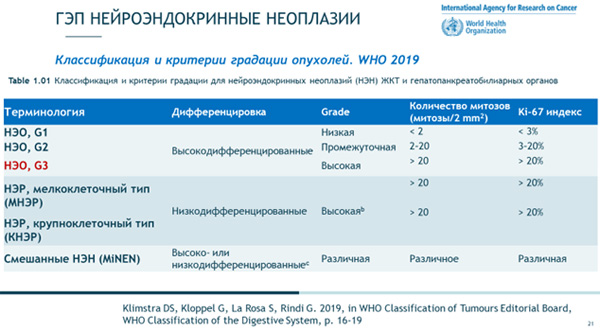
Морфологическая схожесть НЭО не означает идентичность, и безусловно существующая тканеспецифичность нейроэндокринных клеток определяет характерною индивидуальную гормональную продукцию. Окончательный диагноз НЭН должен отражать классификацию опухоли (НЭО или НЭК), степень ее злокачественности (G1, G2, G3), соответствующую TNM-стадию, а также функциональную активность [9].
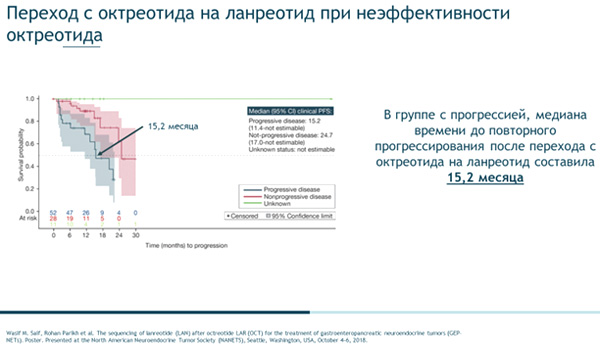
Наряду с классификацией меняются и подходы к медикаментозной терапии. Лекарственная терапия высокодифференцированных НЭО (G1-G2, Ki-67<10%) включает в себя применение аналогов соматостатина (ланреотид и октреотид), интерферонов альфа и их комбинации, а также таргетных препаратов (эверолимуса при любой локализации и сунитиниба при НЭО поджелудочной железы) [10]. Возможности модификации терапии при ее неэффективности приобретают все большее значение. Возможно, поэтому, в последнее время появляется все больше данных о переходе с октреотида на ланреотид при неэффективности терапии ГЭП НЭО. Так, в американском мультицентровом неинтервенционном ретроспективном исследовании изучали эффективность и безопасность ланреотида у пациентов с ГЭП НЭО, которые ранее получали терапию октреотидом не менее 90 дней. Оказалось, что в группе с прогрессией медиана времени до повторного прогрессирования после перехода с октреотида на ланреотид составила 15,2 месяца [11].
А в ретроспективном анализе медицинского центра университета Тафтса также изучили перспективы перевода с одного аналога соматостатина на другой [12]. Основными причинами перевода 16 пациентов с октреотида на ланреотид были: решение пациента (n=6), прогрессирование заболевания (n=6), побочные эффекты (n=2), плохая переносимость (n=1) и дискомфорт/боль при инъекциях (n=1). Снижение уровня ХгА после начала терапии ланреотидом наблюдалось у 15 из 16 пациентов. Ланреотид хорошо переносился пациентами, включая тех, у кого отмечалось прогрессирование заболевания или снижение толерантности к октреотиду.
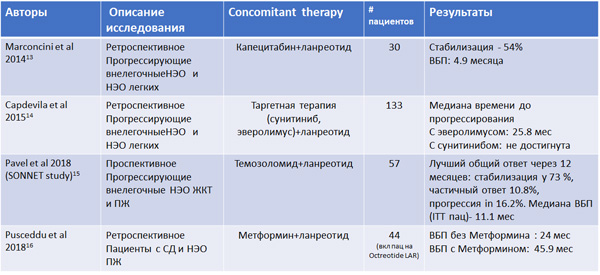
Аналоги соматостатина длительное время применяются в симптоматическом лечении при наличии карциноидного синдрома. Ранее считалось, что влияние аналогов соматостатина ограничено облегчением симптомов и улучшением биохимических показателей, однако рандомизированные контролируемые исследования PROMID и CLARINET с высокой степенью доказательности показали значимый антипролиферативный эффект этой группы лекарственных средств в лечении НЭО. В настоящее время завершен ряд исследований по применению комбинаций АСС с различными группами препаратов, что позволило улучшить ВБП у пациентов с высокодифференцированными НЭО ЖКТ и ПЖ (таблица 2).
Таблица 2
Если вы хотите больше узнать о диагностике и лечении нейроэндокринных опухолей, приглашаем вас посетить информационный проект «Диагностика и тактика ведения пациентов с нейроэндокринными опухолями»: pathologypuzzles.ru/NETs.
Список литературы:
- Lubarsch O. Ueber den primären Krebs des Ileum nebst Bemerkungen über das gleichzeitige Vorkommen von Krebs und Tuberculose. Archiv für pathologische Anatomie und Physiologie und für klinische Medicin. 1888. Т.111, №2, С.280-317.
- Dasari, et al. JAMA Oncol. 2017 Oct 1; 3(10): 1335-1342. doi: 10.1001/jamaoncol.2017.0589.
- Mod Pathol. 2018; 31(12): 1770. Epub 2019 Nov 23.
- Williams ED, Siebenmann RE, Sobin LH & World Health Organization. Histological typing of endocrine tumours. E.D. Williams, in collaboration with R.E. Siebenmann, L.H. Sobin and pathologists in 13 countries. World Health Organization. 1980.
- La Rosa S, Inzani F, Vanoli A, et al. Histologic characterization and improved prognostic evaluation of 209 gastric neuroendocrine neoplasms. Hum Pathol. 2011; 42: 1373.
- Vélayoudom-Céphise FL, Duvillard P, Foucan L, et al. Are G3 ENETS neuroendocrine neoplasms heterogeneous? Endocr Relat Cancer. 2013; 20: 649.
- Lepage C, Ciccolallo L, De Angelis R, et al. European disparities in malignant digestive endocrine tumours survival. Int J Cancer. 2010; 126: 2928.
- Klimstra DS, Kloppel G, La Rosa S, Rindi G. 2019, in WHO Classification of Tumours Editorial Board, WHO Classification of the Digestive System, p. 16-19.
- Bosman FT, Carneiro F, Hruban RH, Theise ND. WHO Classification of Tumours of the Digestive System. 4th ed. International Agency for Research on Cancer (IARC); Lyon, France, 2010.
- Юкальчук Д.Ю. и др. Ланреотид в терапии нейроэндокринных опухолей желудочно-кишечного тракта. Эффективная фармакотерапия. 2016. №8, С.36-41.
- Wasif M. Saif, Rohan Parikh, et al. The sequencing of lanreotide (LAN) after octreotide LAR (OCT) for the treatment of gastroenteropancreatic neuroendocrine tumors (GEP-NETs). Poster. Presented at the North American Neuroendocrine Tumor Society (NANETS), Seattle, Washington, USA, October 4-6, 2018.
- Saif MW, Fu J, Smith MH, Weinstein B, Relias V, Daly KP. Treatment with Lanreotide Depot Following Octreotide Long-Acting Release Among Patients with Gastroenteropancreatic Neuroendocrine Tumors. J Pancreat Cancer. 2018; 4(1): 64-71.
- Marconcini R, et al. Presented at ENETS 2014.
- Capdevila J, et al. BMC Cancer. 2015, 15: 495.
- Pavel M, et al. Presented ay ENETS 2018.
- Pusceddu S, et al. Gastroenterology. 2018, 155: 479-489.




