Молекулярно-биологические изменения при раке молочной железы
Рак молочной железы может быть семейным у 5-10% от общего числа заболевших и спорадическим – у 90-95%.
Для семейного РМЖ характерны наследственно передаваемые мутации генов BRCA1, BRCA2.
BRCA1 располагается в длинном плече 17 хромосомы. В норме белок этого супрессорного гена подавляет пролиферационные сигналы, идущие от эстрогенных рецепторов к клеткам молочной железы. При РМЖ отмечено до 500 мутаций этого гена. Дефекты BRCA1 наблюдаются при наследственном раке в 20%, у 50-85% больных с выявленной мутацией BRCA1 развивается рецепторно отрицательный РМЖ и 15-45% рак яичников.
Супрессорный ген BRCA2 расположен в 13 хромосоме. Его мутации ведут к повышению риска рецепторно положительного РМЖ у женщин и мужчин. Отмечается чаще у лиц старше 50 лет. Повышается риск также РЯ и РПЖ.
Мутации других генов при наследственном РМЖ встречаются реже – это Chek-2, регулирующий в норме переход из одной фазы митотического цикла в другой, супрессорные гены Р53, PTEN, MSHI и MSH2.
Среди особенностей ведения больных с наследственно передаваемыми мутациями генов BRCA1 и 2 строгая диспансеризация и скрининг, двухсторонняя профилактическая мастэктомия.
Спорадический РМЖ – также результат мутационных изменений онкогенов и супрессорных генов, регулирующих процессы клеточного деления.
Нормальный рост молочной железы и ее развитие контролируются сложным взаимодействием многих гормонов и факторов роста. Клетки молочной железы сами секретируют некоторые из них и, таким образом, выполняют аутокринные функции. Кроме того, они экспрессируют рецепторы многих полипептидных факторов и гормонов. Точные биологические процессы, которые возникают в молочной железе и затем являются причиной рака, неизвестны. Ключ к пониманию этих процессов – в изучении жизнедеятельности нормальных клеток. Упомянутые гормоны и факторы роста играют важную роль в клеточном делении и развитии молочной железы, лактации при необходимости, в инвалюционных процессах в ней после прекращения функций.
Эстрогенам придается значение промоторов канцерогенеза в молочной железе. Эстрадиол диффундирует через мембрану в ядро клетки, где связывается с эстрадиоловым рецептором, внося в белок, из которого он состоит, стероидную структуру, затем происходит димеризация 2-х комплексов и соединение с элементом эстрогенного ответа в ДНК. Эти события являются причиной мобилизации других белков, называемых коактиваторами, которые формируют транскрипционный комплекс в ДНК. В последствии РНК полимераза связывается и транскрибируется с мессенджером РНК, несущим сигналы делиться раковым клеткам. Эта информация после попадания в протоплазму клеток передается специфическим белкам – рибосомам.
Эстрогениндуцированные белки регулируют пролиферацию клеток. Под влиянием эстрогенного контроля сами клетки синтезируют и секретируют свои собственные факторы роста, которые оказывают стимулирующее аутокринное и паракринное действие на строму.
Аутокринными факторами роста называются те, которые действуют ускоряюще или замедляюще на клетку? их секретировавшую. Если факторы роста направлены на соседнюю клетку, они являются паракринными.
На рис. 1. представлены схематически разнообразные факторы роста и гормоны, влияющие на клетки молочной железы (в т.ч. и опухолевые).
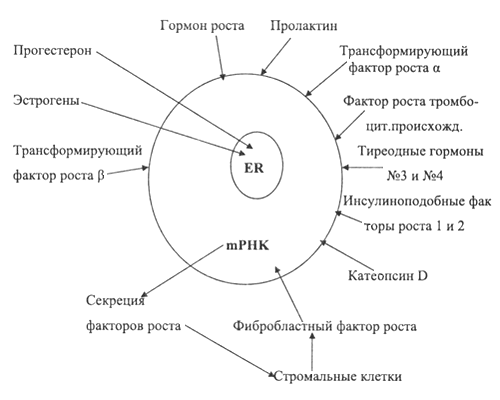
Рис.1. Регуляция деления клетки МЖ (в том числе опухолевой)
Действуют упомянутые факторы роста и гормоны лишь после связывания с соответствующими рецепторами. Гормональные рецепторы находятся в ядрах клеток, рецепторы факторов роста на клеточных мембранах и в цитоплазме. Клетки стромы стимулируют собственную пролиферацию благодаря выделению фибробластного фактора роста и паракринно стимулируют эпителиальные опухолевые клетки. Они могут секретировать инсулиноподобные факторы роста 1 и 2, которые ускоряют пролиферацию эпителиальных клеток. Фактор роста тромбоцитарного происхождения усиливает пролиферацию мезенхиальной стромы раковых опухолей.
Лизосомальный фермент катеопсин Д (урокиназный плазмогенный активатор) помимо митогенного действия на раковые клетки влияет на инвазивность и метастазирование, стимулирует эти процессы. Увеличенная концентрация этого энзима в опухоли связана с неблагоприятным прогнозом.
Особая роль принадлежит трансформирующему фактору роста бета. Этот фактор тормозит деление эпителиальных клеток и, наоборот, стимулирует пролиферацию стромы. От баланса TGF-бета и TGF-альфа зависит злокачественность и агрессивность опухоли.
Многочисленные экспериментальные данные показывают, что чрезмерная экспрессия онкогенов – в прошлом нормальных генов – может привести к глубоким изменениям роста и гомеостаза нормального эпителия. Среди экспрессированных онкогенов – рецепторы фактора роста Her2/neu (erb-2), Her3, Her4, члены семейства myc и ras. В норме эти гены регулируют пролиферацию и развитие молочной железы. Гиперэкспрессия онкогенов является предполагаемой причиной индукции рака молочной железы. Существуют прямые экспериментальные доказательства их определяющей роли в генезе опухолей. Внедрение генов myc, ras, Her2 в молочные железы трансгенных мышей приводит к развитию в них раковых опухолей.
В связи с гиперэкспресией или мутацией онкогенов клетки получают гиперстимуляционные сигналы для деления. В норме существует баланс негативных и позитивных мессенджеров РНК. При повреждении ДНК до ее регенерации супрессорные гены с помощью белков сдерживают пролиферативные процессы. В опухолях ингибирующие функции таких генов как Р53, RB1, BRSA1 и 2 подавлены. В результате функциональной или химической деактивации супрессорных генов вместо регуляции деления клеток наступает расстроенный транзит опухолевых клеток через различные фазы цикла.
Развитие microarray технологии позволило охарактеризовать генный профиль многих злокачественных новообразований, в том числе и РМЖ. Кроме общих закономерностей упомянутая технология дает возможность расшифровать отличия генного портрета опухоли у разных больных. Ретроспективные сопоставления генетических находок с клиническим течением, ответом на терапию, сроками выживания вооружают онкологов информацией, которая ляжет в основу нового важнейшего принципа лечения больных – генетически обоснованной персонализации. Первые шаги уже сделаны. Наблюдаемая гиперэкспрессия генов семейства erbB является основанием для применения молекулярного ингибитора лапатиниба. Гиперэкспрессия VEGFR2 (рецептор васкулярно-эндотелиального фактора роста 2) означает, что больным в пременопаузе следует сочетать адъювантное лечение тамоксифеном в комбинации с ингибиторами этого сосудистого фактора роста и т.д.
По монографии А.М. Гарина, И.С. Базина
«Десять наиболее распространенных злокачественных опухолей»,
г. Москва, 2006




