МРТ в оценке прогноза эффективности предоперационной химиолучевой терапии у больных раком шейки матки
Рубцова Н.А. 1, Бойко А.В. 2, Демидова Л.В. 2, Андреева Ю.Ю. 3, Данилова Н.В. 3
ФГБУ «Московский научно-исследовательский институт им. П.А. Герцена» Минздравсоцразвития России, 125284, Москва, 2-й Боткинский проезд, д. 3
1) отделение рентгенодиагностики,
2) отделение лучевой терапии,
3) патоморфологическое отделение.
Сведения об авторах:
Рубцова Наталья Алефтиновна, кандидат медицинских наук, руководитель отделения рентгенодиагностики диагностического отдела, раб. тел.: 8(495) 945-59-39
e-mail:
Бойко Анна Владимировна, доктор медицинских наук, профессор, руководитель отделения лучевой терапии
Демидова Людмила Владимировна, доктор медицинских наук, старший научный сотрудник отделения лучевой терапии
Андреева Юлия Юрьевна, доктор медицинских наук, ведущий научный сотрудник патоморфологического отделения
Данилова Наталья Владимировна, клинический ординатор патоморфологического отделения
Реферат
Целью исследования являлось определение возможности прогнозирования эффективности предоперационной химиолучевой терапии у пациенток с инвазивными формами рака шейки матки на основе перфузионных характеристик опухоли по данным динамической магнитно-резонансной томографии.
Материалы и методы. В исследование включены 43 больные раком шейки матки, из них в 92% случаев стадия процесса соответствовала IIB-IIIB (FIGO), гистологическая форма опухоли у 93% пациенток была представлена плоскоклеточным раком. Для стадирования опухолевого процесса и оценки эффективности предоперационной химиолучевой терапии в предоперационном периоде всем больным дважды проводилась МРТ с внутривенным контрастным динамическим усилением с последующей оценкой показателей перфузии.
Результаты. При анализе суммарных графических отображений динамического контрастирования до химиолучевой терапии и данных послеоперационных гистологическогих исследований, установлена корреляционная связь между уровнем гетерогенности перфузии и степенью лечебного патоморфоза. В случаях, когда гетерогенность перфузии не превышала 10% отмечался хороший эффект неоадьювантной терапии, сопровождающийся IV степень лечебного патоморфоза в опухоли. При колебаниях гетерогенности перфузии от 10 до 20% эффект лечения соответствовал II-III степени лечебного патоморфоза. В случаях гетерогенности перфузии превышающей 20% отмечалась низкая эффективность лечения предоперационной химиолучевой терапии.
Выводы. Полученные результаты исследования свидетельствуют о возможности прогнозирования эффективности химиолучевого лечения у больных раком шейки матки по данным перфузионной МРТ.
Ключевые слова: МРТ, рак шейки матки, предоперационная химиолучевая терапия, оценка эффективности, прогноз эффективности.
MRI in the evaluation of forecast efficiency neoadjuvant
chemoradiation therapy in patients with cervical cancer
Rubtsova N.A.1, Boyko A.V.2, Demidova L.V.2, Andreeva YU. YU.3, Danilova N.V.3
Federal State Department "Hertzen Moscow Research Cancer Institute" Ministry of Health and Social Development of the Russian Federation. 3, 2-nd Botkinsky Proyezd, 125284, Moscow, Russia
1) Department of Radiography,
2) Department of Radiotherapy,
3) Department of Pathomorphology
Abstract
Objective of research was definition of possibility prognosing of efficiency neoadjuvant chemoradiation therapy (n-CRT) at patients with cervical cancer invasive forms based on perfusion tumor characteristics at a magnetic resonance imaging tomography (MRI) with dynamic intravenous contrast enhancing.
Materials and Methods: 43 patients with cervical cancer invasive forms are examinated, the majority patients with stage IIB-IIIB (FIGO), histologically at the majority (93 %) – plane cells cancer. For the definition of local staging cervical cancer all patient were examinated by MRI with intravenous contrast dynamic enhancing (with subsequent estimation of perfusion indicators) before and two weeks after n-CRT in the preoperative period.
Results of the analysis graphic displays of dynamic contrasting before n-CRT and given postoperative histological materials, correlation connection between level of heterogeneity of perfusion and degree of a tumour pathomorphosis is established. In cases when heterogeneity doesn't exceed 10 % good efficiency n-CRT (IV degree tumour pathomorposis) is marked. At heterogeneity fluctuations in a tumor of 10-20 % efficiency of treatment average (II-III degree tumour pathomorposis), and at high values of heterogeneity perfusion in a tumor (more than 20 %) efficiency n-CRT has appeared low.
Conclusions: The received results of research testify the possibility of prognosing efficiency of n-CRT at patients with cervical cancer based on perfusion data, calculated at MRI with dynamic contrast enhancing.
Key words: MRI, cervical cancer, neoadjuvant chemoradiation therapy, estimation efficiency, prognosing efficiency.
Введение
Рак шейки матки (РШМ) занимает второе место в структуре женской заболеваемости России среди злокачественных опухолей половых органов и является одной из доминирующих причин женской смертности [1]. Большинство онкологических центров отдают предпочтение хирургическому подходу в лечении РШМ на стадиях Ia1- IIA [2, 3]. В свою очередь, лечение пациенток с инвазивным РШМ, при наличие распространения опухоли в параметральную клетчатку (стадия FIGO IIB) принято начинать с лучевой терапии. Показаниями к назначению предоперационной химиолучевой терапии служат: наличие экзофитной опухоли больших размеров, выход опухоли в параметральную клетчатку, наличие метастазов в тазовые лимфатические узлы. Используемые 5-фторурацил и препараты платины в комбинации с лучевой терапией позволяют повысить эффективность проводимого лечения [4, 5, 6]. В ряде случаев, проводимая в предоперационном этапе химиолучевая терапия позволяет не только уменьшить объем и распространенность процесса, но и полностью девитализировать опухоль, что проявляется IV степенью лечебного патоморфоза, установленного при морфологическом исследовании после выполнения расширенной экстирпации матки. Безусловно, заключительно оценить эффективность проведенного исследования позволяет исключительно гистологическое исследование. Однако информация о результатах проводимой терапии хирургам необходима на дооперационном этапе, чтобы иметь возможность адекватно спланировать объем предстоящего вмешательства.
В современной практике для определения реакции опухоли на химиолучевую терапию используются методы лучевой диагностики, такие как: ультразвуковое исследование (УЗИ), рентгеновская компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). Все эти диагностические методы (в большей степени УЗИ и МРТ, что обусловлено их физическими принципами и как следствие возможностями тканевой визуализации) позволяют регистрировать изменения распространенности процесса, относительно первичной опухоли и метастазов в тазовых лимфатических узлах, включая численные изменения их объемов. Однако волюметрический анализ не всегда позволяет получить достоверную картину о наличие остаточной опухоли [6]. Зачастую бывает крайне затруднительно определить остаточную опухоль на фоне реактивных изменений. С этой целью возможно проведение доплеровского картирования и МРТ с динамическим контрастным усилением, дающих возможность определять зоны патологической васкуляризации. При сопоставлении этих двух методов бесспорным преимуществом обладает МРТ, во-первых в силу лучшей визуализации зон локорегионарного лимфооттока (в т.ч. обтураторных областей), во-вторых из-за возможности получения количественной оценки перфузии в исследуемой области.
В последнее время был опубликован ряд работ, демонстрирующих возможность динамической МРТ в оценке распространенности РШМ, прогнозе течения заболевания и прогнозе эффективности химиолучевой терапии [8, 9, 10, 11].
В отделении рентгенодиагностики диагностического отдела ФГУ «МНИОИ им. П.А. Герцена» Минздравсоцразвития России была предпринята попытка разработать МР-предикторы эффективности наряду с определением возможностей МРТ в оценке эффективности химиолучевой терапии на основе изучения перфузионных свойств опухоли, в сопоставлении с результатами послеоперационного морфологического исследования.
Материалы и методы
Для реализации поставленных задач было обследовано 43 больные инвазивным РШМ, в возрасте от 24 до 44 лет (средний возраст составил 34 года), проходившие лечение в клиниках ФГУ «МНИОИ им. П.А. Герцена» Минздравсоцразвития России в период с декабря 2007г. по июль 2011г. Всем пациенткам на первом этапе лечения выполнялась лапароскопическая транспозиция яичников; второй этап включал проведение неоадьювантной химиолучевой терапии; третий этап заключался в расширенной экстирпации матки.
В 11 случаях, основываясь на клинической ситуации (с учетом прогностических факторов: гистотип, степень дифференцировки, распространенность опухоли), было рекомендовано продолжить лечение в объеме адьювантной полихимиотерапии, и дополнительно в 1-м случае – дистанционной лучевой терапией на парааортальную область. Химиолучевая терапия проводилась по схеме: в течение 5 дней внутривенно введение 5-фторурацил по 350 мг/м2, после двухдневного перерыва начинают дистанционную лучевую терапию по схеме динамического фракционирования дозы.
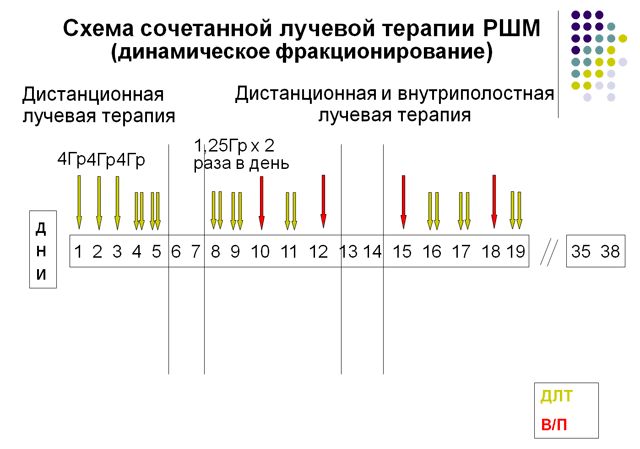
Первые 3 дня подводят укрупненные фракции (4 Гр) в сочетании с одновременным введением препаратов платины по 20 мг/м2. В дальнейшем облучение продолжают в режиме гиперфракционирования с разовой очаговой дозой (РОД)=1,25Гр х 2 раза в день с интервалом 4-5 часов, (дневная доза 2,5Гр), до суммарной очаговой дозы (СОД)=40-50 Гр. При сочетанной лучевой терапии дистанционное облучение чередуют с сеансами внутриполостной гамма-терапии
(схема 1).
Большинство случаев 40 (93%) были представлены плоскоклеточным раком, из них 25 (62.% %) – с низкой степенью дифференцировки, 13 (32.5 %) – умереннодифференцированный плоскоклеточный рак и 2 (5 %) – высокодифференцированный. Анализ больных в соответствии со стадией процесса представлен в таблице 1.
Таблица 1
Распределение больных в соответствие с TNM классификацией РШМ
| Количество больных n (%) | Стадия опухолевого процесса |
|---|---|
| 1 (2.33 %) | T1b1N1M0 |
| 3 (6.98 %) | T1b2N0M0 |
| 4 (9.30 %) | T1b2N1M0 |
| 16 (37.21 %) | T2bN0M0 |
| 8 (18.60 %) | T2bN1M0 |
| 6 (13.95 %) | T2aN0M0 |
| 2 (4.65 %) | T3bN0M0 |
| 2 (4.65 %) | T3bN1M0 |
| 1 (2.33 %) | T3bN0M1 |
Большинство составили пациентки со стадией IIB (FIGO), т.е. с распространением опухоли в параметральную клетчатку. У 15 больных имелось метастатическое поражение внутритазовых лимфатических узлов, в 1-м случае был выявлен метастаз в парааортальный лимфоузел.
Всем больным МРТ органов малого таза выполнялась дважды: на диагностическом этапе, для уточнения распространенности опухолевого процесса; и после проведения химиолучевого лечения, в предоперационном периоде с целью оценки его эффективности. МР-исследование органов малого таза проводилось на 1.5Т МР-томографе Titan Vintage (Toshiba MS). Протокол МР-исследования органов малого таза представлен в таблице 2.
Таблица 2
Протокол МР-исследования малого таза при раке шейки матки
| Последовательность, взвешанность и ось сканирования |
TR | TE | FOV (см) | MTX | ST (мм) | GAP | NAQ |
|---|---|---|---|---|---|---|---|
| Sag T2 FSE 2D | 6433 | 90 | 28,0x28,0 | 224х320 | 4,0 | 5,0 | 1,0 |
| Ax T2 FSE 2D | 7600 | 100 | 43,0x32,0 | 320х384 | 5,0 | 0,6 | 1,0 |
| Cor T2 FatSat FSE 2D | 4776 | 160 | 40,0x30,0 | 256х384 | 5,0 | 0,5 | 1,0 |
| Obl AX T2 (перпендикулярно цервикальному каналу) FSE 2D | 5600 | 80 | 25,0x25,0 | 224х288 | 3,0 | 1,0 | 1,0 |
| Obl Cor T2 (параллельно цервикальному каналу) FSE 2D | 5600 | 80 | 25,0x25,0 | 224х288 | 3,0 | 1,0 | 1,0 |
| Cor T1 SE 2D | 621 | 15 | 40,0х37,0 | 288х288 | 6,0 | 1,0 | 1,0 |
| Dynamic 3D FatSat | 5 | 2,5 | 30,0х25,0 | 192х256 | 4,0 | 1,0 | 1,0 |
Проведение динамической МРТ состояло из двух сегментов: первый – нативное сканирование; второй - с внутривенным введением контраста (Gd-DTPA) из расчета 0.1ммоль/кг, с числом повторений – 5 и задержкой по 10.0 сек., время каждого повторения составляло 27.6 сек.
Для изучения возможностей динамической МРТ в оценке остаточной опухоли в предоперационном периоде, через 2 недели после проведения химиолучевого лечения, в проекции ранее визуализируемой опухоли проводилась оценка перфузии, с построением ее графических отображений. Полученные данные сопоставлялись с исходными показателями перфузии в опухоли (до проведения химиолучевой терапии) и для контроля сравнивались с уровнем перфузии в неизмененной строме шейки матки.
Для исследования влияния перфузионных свойств опухоли на эффективность химиолучевого лечения выполнялось построение графических отображений динамического контрастного усиления с измерением количественного отображения перфузии во всем объеме новообразования. Для этого на сагиттальных постконтрастных изображениях, включая каждый уровень, где выявлялись опухолевые массы, обводилась зона интереса (площадь опухолевого поражения), с последующим определением в ней показателей перфузии. Далее выполнялось графическое построение кривой, отражающей накопление контраста в опухоли в зависимости от времени.
Количество кривых соответствовало количеству срезов, проходящих через опухоль. Для оценки однородности перфузии в опухоли производилось совмещение всех кривых, с последующим анализом разброса значений и вычисления процентного соотношения гетерогенности. Для этого максимальное значение принималось за 100%, исходя из чего вычислялось процентное соотношение минимального значения, с последующим определением разницы между ними, которая и отражала уровень гетерогенности. Данное исследование производилось дважды, с целью сопоставления исходных значений с показателями, полученными после химиолучевого лечения.
Результаты
При проведении анализа МРТ с динамическим контрастным усилением и последующим определением показателей перфузии в оценке остаточной опухоли все пациентки были подразделены в две группы: 1-ю составили 34 больные с наличием остаточной опухоли, определяемой на Т2 взвешенных изображениях (ВИ); 2-ю – 9 пациенток с отсутствием визуальных признаков опухолевого роста. В обеих группах после проведенной химиолучевой терапии отмечался подъем уровня перфузии относительно исходных значений, при этом уровень повышения не зависел от первоначальных показателей.
Проанализировав 2-ю группу пациенток было установлено, что в проекции ранее определяемой опухоли (в зоне сохраняющегося умеренно повышенного МР-сигнала на Т2 ВИ) на постконтрастных Т1 ВИ отмечалось накопление контраста, визуально идентичное неизмененной строме. Однако при построении графиков зависимости динамического контрастирования во всех 9 случаях регистрировалась существенная разница пиковых значений. В зоне ранее определяемого новообразования интенсивность накопления была всегда выше, что затрудняло дифференциальную диагностику между остаточной опухолью и реактивными изменениями на проведенную химиолучевую терапию.
Сопоставив результаты вольюметрического анализа опухоли, данные послеоперационного гистологического исследования и суммарные графические отображения динамического контрастного усиления до и после химиолучевого лечения, было выделено три группы больных, в зависимости от значений гетерогенности перфузии (табл. 3).
Таблица 3
Зависимость эффективности химиолучевой терапии
от уровня гетерогенности перфузии в опухоли
| Уровень эффективности ХЛТ | Высокая эффективность | Средний эффект | Низкая эффективность |
| Гетерогенность перфузии в опухоли (%) |
до 10 % | от 10 % до 20 % | более 20 % |
В случаях, когда гетерогенность не превышала 10% отмечалась хорошая эффективность химиолучевой терапии, с выраженным уменьшением объема опухоли, до полной ее резорбции, что подтверждалось морфологическим заключением и соответствовало IV степени лечебного патоморфоза (график 1, рис. 1 а, б).
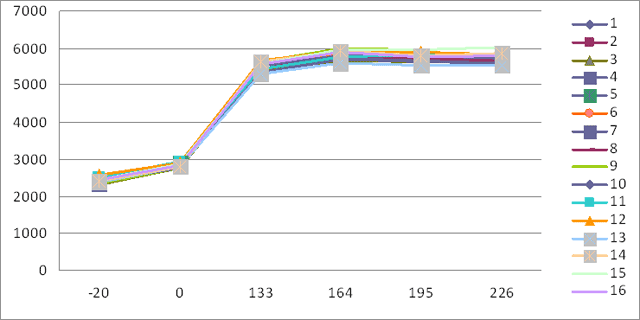
График 1. Перфузия в опухоли шейки матки с низким показателем гетерогенности (гетерогенность соответствует 5%).
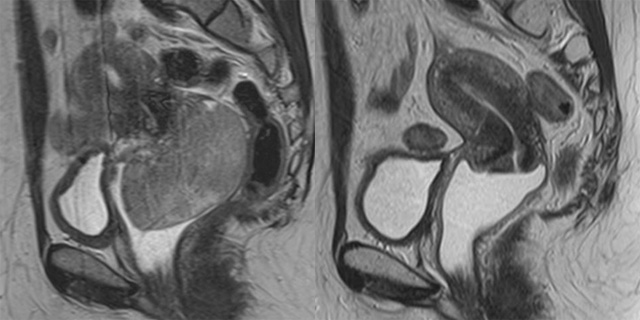
Рисунок 1 а, б – МР-томограмма органов малого таза у больной раком шейки матки.
Т2 ВИ в сагиттальной проекции до и после проведения неоадьювантной химиолучевой терапии (полная резорбция опухоли).
Средняя эффективность лечения, соответствующая II – III степени лечебного патоморфоза, установлена при колебаниях гетерогенности в пределах от 10% до 20%. Низкая эффективность неоадьювантной химиолучевой терапии была отмечена у больных с высокими значениями гетерогенности перфузии в опухоли, превышающей 20% (график 2, рисунок 2 а,б).
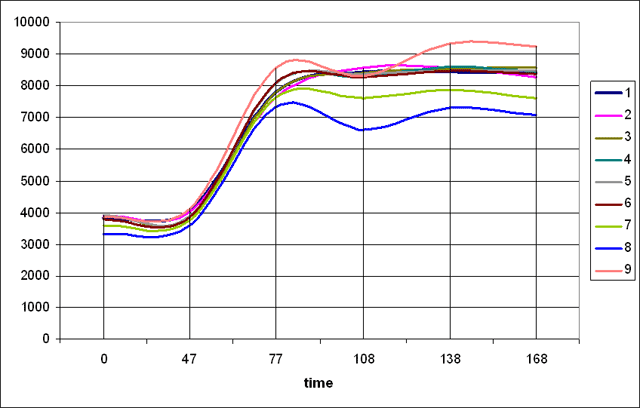
График 2. Перфузия в опухоли шейки матки с высоким показателем гетерогенности (гетерогенность соответствует 25%).
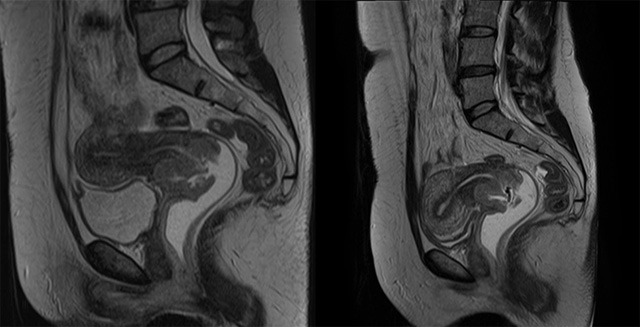
Рисунок 2 а, б – МР-томограмма органов малого таза у больной раком шейки матки.
Т2 ВИ в сагиттальной проекции до и после проведения неоадьювантной химиолучевой терапии.
Гетерогенность перфузии не зависела от степени дифференцировки опухоли. Во всех случаях после проведения химиолучевого лечения, в сравнении с исходными данными, наряду с повышением значений перфузии отмечалось снижение гетерогенности
(график 3а, б).
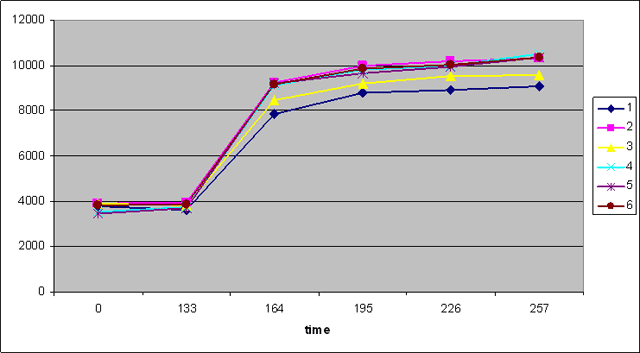
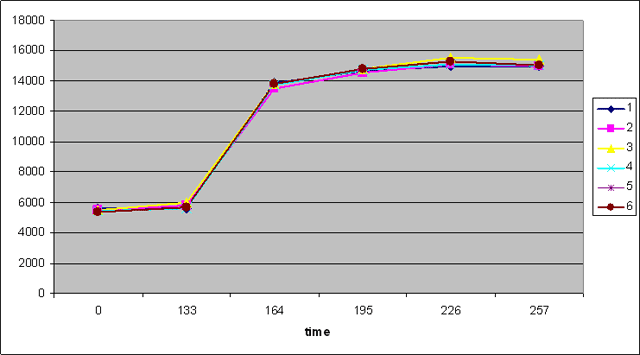
График 3 а, б. Перфузия в опухоли шейки матки до и после проведения химиолучевой терапии – снижение гетерогенности перфузии (а - до лечения гетерогенность составила 13%, б – после лечения гетерогенность соответствует 6%).
Заключение
Полученные результаты исследования свидетельствуют о возможности прогнозирования эффективности химиолучевого лечения у больных местнораспространенными формами РШМ на основании данных перфузии, вычисленных при МРТ с динамическим контрастным усилением. Определение достоверных корреляционных связей между показателями
МР-перфузии в опухоли до начала неоадьювантной терапии и степенью лечебного патоморфоза по результатам послеоперационного морфологического исследования позволит разработать критерии прогноза эффективности лечения, что будет способствовать индивидуализации и оптимизации подходов при выборе лечебной тактики. В связи с этим данная работа является перспективной и требует продолженного детального изучения и разработки предикторов эффективности на большем количестве наблюдений.
Список литературы
- Руководство по онкологии (Под редакцией В.И. Чиссова, С.Л. Дарьяловой). - М.: МИА. 2008; 518-540.
- Лекции по онкогинекологии (Под редакцией М.И. Давыдова, В.В Кузнецова). – М.: «МЕДпресс-информ», 2009; с. 199-284.
- DiSaia P.J., Creasman W.T. Clinical gynecologic oncology – 7-th ed. Mosby Elsevier – 2007; P.812.
- Morris M., Eifel P.J., Lu J. et al. Pelvic radiation with concurrent chemotherapy compared with pelvic and para-aortic radiation for high-risk cervical cancer. N. Engl. J. Med. – 1999; №340: P.1137-1143.
- Rose P.G., Bundy B.N., Watkins E.B. et al. Concurrent cisplatin based radiotherapy and chemotherapy for locally advanced cervical cancer. N. Engl. J. Med. – 1999; № 340: P.1144-1153.
- Keys H.M., Bundy B.N., Stehman F.B et al. Cisplatin, radiation, and adjuvant hysterectomy compared with radiation and adjuvant hysterectomy for bulky stage IB cervical carcinoma. N.Engl. J. Med. – 1999; №340 – P.1154-1161.
- Wagenaar H.C. et al. Tumour diameter and volume assessed by MRI in prediction of outcome for invasive cervical cancer. Gynecol. Oncol. – 2001; №82 – P.474-482.
- Seki H., Azumi R, Kimura M. et. al. Stromal invasion by carcinoma of cervix: Assessment with dynamic MR imaging. AJR – 1997; №168 – P.:1579-1585.
- Postema S., Pattynama P., van Rijswijk C., Trimbos B. Cervical Carcinoma: Can Dynamic Contrast-enhanced MRI Help Predict Tumor Aggressiveness? Radiology – 1999; №210 – P.217-220.
- Hulse P., Carrington B. MRI manual of pelvic cancer. - London and New York: Martin Dunitz Taylor & Francis group. 2004; P.256.
- Mayr N., Yuh W., Jajoura D. Ultra Early Predictive Assay for Treatment Failure Using Functional MRI and clinical Prognostic Parameters in Cervical Cancer. A. J. R. 2010; V. 116: P.903-912.

