Современное состояние проблемы использования
большого сальника в качестве аутотрансплантата
при маммопластике у больных раком молочной железы
Пак Д.Д., Трошенков Е.А., Усов Ф.Н., Петровский Д.А.
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена», Москва, Россия
Опубликовано: Журнал «Онкохирургия», 2012, том 4, №4.
В обзоре литературы рассмотрены достоинства и недостатки использования лоскута большого сальника в качестве аутотрансплантанта у больных раком молочной железы.
Материал и методы. История использования большого сальника в качестве пластического материала насчитывает более 100 лет. Вначале был предложен забор сальника открытым способом. Однако появление дополнительного рубца на передней брюшной стенке ограничивало применение данной методики. В конце 90-х годов с развитием эндоскопической хирургии появилась возможность забора сальника с применением лапароскопической техники. Предпосылкой к этому стала детальное изучение особенностей сосудистой архитектоники, иннервации, биохимических и микрофизиологических особенностей большого сальника. В литературе освещается определённый круг методов забора сальника в зависимости от локализации опухоли в различных квадрантах молочной железы. Были разработаны различные варианты для обширной мобилизации сальника, соответствующие вариантам прохождения артерий сальника и связывающей их сосудистой сети. Предпочтение отдаётся сальниковому лоскуту на правых желудочно-сальниковых артериях. Преимущество трансплантата на основе большого сальника в том, что его тканевая масса хорошо кровоснабжается, и её объём достаточен для формирования выпуклой молочной железы. Однако авторы обращают внимание на возникновение осложнений в 10 и более процентах наблюдений. В то же время нельзя недооценивать и барьерную роль большого сальника в брюшной полости. Авторы отмечают также длительность и сложность операции, обусловленные наличием абдоминального этапа, опасностью внутрибрюшного кровотечения, обнаружением спаек брюшной полости. Применение свободного лоскута большого сальника требует также владения микрохирургической техникой.
Выводы. Однако лёгкая мобилизация, прекрасная пластичность и богатое кровоснабжение определяют хорошую перспективу использования большого сальника для восполнения объёма молочной железы после различных вариантов подкожной мастэктомии. При выборе данного хирургического метода необходима сравнительная оценка степени травматичности оперативного вмешательства и риска развития осложнений в связи с удалением небезразличного для брюшной полости органа.
Ключевые слова: подкожная мастэктомия, первичные реконструктивные операции, рак молочной железы, лоскут большого сальника.
Совершенствование диагностической онкологической службы и использование современных достижений в клинике позволяют добиться заметного улучшения результатов лечения больных раком молочной железы. В этой ситуации приоритетными становятся органосохраняющие операции и обеспечение хорошего качества жизни женщин. Последнее предполагает адекватную социально-медицинскую реабилитацию и, в первую очередь, косметический эффект после операции.
Проблема восстановления формы молочной железы после различных видов мастэктомий и обширных резекций в последние годы становится все более актуальной. Ежегодно в России и других странах мира обращаются в специализированные центры для решения вопроса о восстановительной операции около 110000-220000 тыс. больных.
Современный арсенал способов улучшения эстетических результатов реконструкции молочной железы крайне обширен. Их можно разделить на две группы: реконструкция молочной железы с использованием синтетических материалов (эспандеров и имплантов) и реконструкция с использованием собственных тканей [1]. К первой группе можно отнести двухэтапные операции с первичной дермотензией экспандером и последующей имплантацией эндопротеза [2]. Другую группу составляют реконструктивные операции с использованием перемещенных на сосудистой ножке или свободных аутотрансплантатов из мышц или сальника. Возможно также сочетание этих методик, т.е. использование собственных тканей в сочетании с имплантатом [3-6]. Трудности в восстановлении формы молочной железы после мастэктомии обусловлены отсутствием резерва кожи, грудных мышц, у некоторых больных – наличием грубой рубцовой деформации в этой области [7].
Основными материалами для реконструкции за счет собственных тканей являются поперечный лоскут прямой мышцы живота, торокодорзальный лоскут, ягодичный лоскут [8-10]. В настоящее время число различных видов кровоснабжаемых аутотрансплантатов, широко используемых в клинической практике, превышает 60 [11].
Пластические свойства большого сальника, являющегося поливалентной тканью, известны давно: он используется для решения большого спектра реконструктивных проблем [12, 13]. Немецкий хирург V. Das [14] на основании измерений, выполненных на 200 трупах и 100 пациентах в ходе лапаротомии, определил среднюю длину большого сальника в 25 см, среднюю ширину – в 33 см (у женщин эти размеры на 1-2 см меньше). Большой сальник состоит из двойного листка брюшины, сложенного таким образом, что образуется хорошо кровоснабжаемая четырехслойная структура, содержащая варьирующее количество жира. Передний листок отходит от большой кривизны желудка и начальной части двенадцатиперстной кишки. Он ложится поверх брюшных внутренностей, закрывая их на разном протяжении, а затем складывается назад и поднимается до поперечно-ободочной кишки. Сальник получает кровоснабжение от правой и левой желудочно-сальниковых артерий, которые, объединяясь, образуют желудочно-сальниковую аркаду вдоль большой кривизны желудка. При заборе лоскута обычно основываются на правых желудочно-сальниковых сосудах. Существуют различные варианты прикрепления правого края сальника: он может начинаться от восходящей ободочной кишки, двенадцатиперстной кишки или свободно свисать от пилорического отдела желудка. Последний случай представляет предпочтительный анатомический вариант [15-17].
Преимущества использования большого сальника при дефектах мягких тканей, образовавшихся после удаления новообразования, заключаются в его возможностях обеспечивать дополнительное кровоснабжение, уменьшать воспалительный процесс, заполнять полости, остающиеся после удаления тканей, ускорять заживление [18]. Используя большой сальник, в ходе одной технически несложной операции может быть получен лоскут размером почти 200 см3, состоящий из хорошо васкуляризированной клеточной массы, содержащей и жировую ткань, который легко можно переместить на воспринимающее ложе, обеспечив реваскуляризацию кожного трансплантата средней толщины [17].
Были разработаны различные варианты обширной мобилизации сальника, соответствующие вариантам прохождения артерий сальника и связывающей их сосудистой сети. В 1963 I. Kiricuta впервые предложил перемещать большой сальник на грудную стенку для закрытия дефектов кожи [19, 20]. Он считал, что сальник может быть перенесен на грудную стенку без мобилизации, а с точки зрения мобилизации рассматривал обе желудочно-сальниковые артерии как равноценные. M. Abbes и соавт [21] отдавали предпочтение правой желудочно-сальниковой артерии. K. Harii [22, 23] переносил на переднюю грудную стенку свободный лоскут большого сальника с питающей ножкой и анастомозировал ее с сосудами латеральной поверхности груди.
J. Fissette [24] видел преимущество трансплантата на основе большого сальника в том, что его тканевая масса хорошо кровоснабжается, и ее объем достаточен для формирования хорошо выпуклой молочной железы. С 80-х гг. производились попытки комбинирования пересадки большого сальника с применением протеза, если сальник не обеспечивал достаточного объема молочной железы [25, 26].
В подавляющем большинстве работ как единственно возможный оперативный доступ к сальнику для формирования сальникового лоскута и обеспечения хорошей экспозиции рассматривается лапаротомия. Однако она сама является травматичным вмешательством и несет опасность возникновения осложнений в послеоперационном периоде (нагноение операционной раны, развитие послеоперационных грыж, спаечной болезни) [27].
Анализируя недостатки свободной трансплантации, R. Fridman (1985) отметил довольно сдержанное отношение к ней даже опытных хирургов. Такая операция требует особых материалов, аппаратуры и инструментария, специально подготовленных бригад. Сама операция, длящаяся 8-10 и более часов, не лишена определенного риска, случаи неудач составляют 10% и более [28]. D. Hidalgo и соавт. [29], исходя из десятилетнего опыта 716 свободных трансплантаций, отмечают неудачи в 30% клинических наблюдений. По данным работы C. Contant [30], полный или частичный некроз при свободной трансплантации кожи на большой сальник при пластических операциях на молочной железе наблюдался в 35%, что потребовало повторных реконструктивных вмешательств.
Высокая травматичность оперативных вмешательств с использованием лоскута большого сальника, связанная с необходимостью выполнения лапаротомии для его выделения, ограничила его применение в практической онкологии и пластической хирургии. В онкохирургии первые сообщения об эндохирургически-ассистированных вмешательствах с созданием искусственной полости относят к 1996 г., когда была описана методика аксиллярной лимфодиссекции с использованием лапароскопа [31, 32].
Экспериментальные и клинические данные показывают, что сальник может быть успешно забран как свободный лоскут под лапароскопическим контролем [33]. Макро- и микроскопические исследования подтверждают жизнеспособность этого подхода. Если сальник не требуется полностью, можно безопасно забрать его лоскут, соответствующий размерам дефекта, оставив только небольшой рубец на животе. Процедуру и послеоперационный период пациенты переносят хорошо. Разработка малоинвазивного способа формирования сальникового лоскута и эндохирургического перемещения его на область удаленной молочной железы способствовала улучшению косметических результатов у данного контингента больных [34].
R. Saltz и соавт. [35] успешно выполнили лапароскопически-ассистированный забор сальника у пациента для закрытия мягкотканного дефекта нижней конечности. Сальник был обследован лапароскопически, а затем выведен внебрюшинно для диссекции. Авторы отмечают, что полностью внутрибрюшная диссекция большого сальника сложна и не выполняется. Его сложнее забрать, чем тощую кишку или прямую мышцу живота, так как он хорошо кровоснабжен и очень подвижен.
Использование эндоскопических технологий при одномоментной или отсроченной реконструкции молочной железы обеспечивает ряд неоспоримых преимуществ: уменьшение послеоперационных рубцов, хорошую визуализацию и, как следствие, адекватный гемостаз и снижение травматичности вмешательства [36-38]. Уменьшение боли обеспечивается малыми разрезами прецизионного вмешательства, более легким течением послеоперационного периода. I. Cothier-Savey [39] применил эндохирургическую технологию при одномоментной реконструкции молочной железы лоскутом большого сальника 10 больным. Ни у одной больной не возникло осложнений после данной операции. Послеоперационные рубцы были минимальны (рис. 1, 10). Число дней пребывания в стационаре сократилось до 7.

Рис. 1. Схема введения троакаров для лапароскопического выделения лоскута большого сальника.

Рис. 10. Вид послеоперационной раны передней брюшной стенки после лапароскопической мобилизации лоскута большого сальника.
В целом, эндоскопические доступы сопровождаются снижением осложнений воспалительного характера за счет ограниченного контакта области операции с окружающей средой и, как следствие, уменьшения контаминации. По данным Я.М. Долгиной [40], применение эндохирургических технологий при реконструкции молочной железы позволяет сократить осложнения воспалительного характера в 2 раза по сравнению с традиционными операциями (2,8% и 5,8% соответственно), а осложнения, связанные с приживляемостью перемещенных лоскутов, – в 5 раз. Применение эндовидео-ассистированных методик позволило также улучшить косметические результаты оперативного вмешательства.
Последние данные по применению эндохирургической технологии в одномоментной реконструкции молочной железы с использованием большого сальника опубликовали японские исследователи H. Zaha и соавт. [41]. В результате лечения 44 больных они наблюдали незначительное количество осложнений: повреждение сосуда большого сальника отмечено у одного больного (2,3%), инфекционные осложнения трансплантата или послеоперационной раны – у 4 больных (9,1%), эпигастральная грыжа – у одного (2,3%). Косметический эффект во всех случаях был наилучший. Авторы подчеркивают целесообразность предпочтения пластики лоскутом большого сальника у пациенток с небольшим (0-2) размером молочных желёз по чашечкам бюстгальтера и локализации опухоли в нижнемедиальных квадрантах молочных желёз [42, 43].
Важным моментом является определение показаний к малоинвазивному методу забора пластического материала. Выбор аутопластического материала для контурной коррекции молочной железы после органосохраняющей операции должен основываться на локализации первичной опухоли: при расположении опухоли в медиальных квадрантах оптимальным является лоскут большого сальника, при латеральном расположении – лоскут широчайшей мышцы спины. По мнению А.Л. Владыкина [44], комфортно использовать лоскуты большого сальника можно только при пластике нижних квадрантов молочной железы, т.к. высокое перемещение васкуляризированного лоскута сальника приводит к его избыточному натяжению. При этом правосторонний лоскут большого сальника целесообразно использовать в нижних квадрантах правой молочной железы, нижне-внутреннем квадранте левой молочной железы, левосторонний – в нижне-наружном квадранте левой молочной железы, куда не дотягивается правый лоскут. Основные негативные моменты при использовании левых желудочно-сальниковых сосудов заключаются в том, что левые желудочно-сальниковые сосуды уже и короче (длина 14-25 см), чем правые (25-31 см), поэтому лоскут сальника получается более коротким и содержит меньше ткани. Кроме того, близость желудочно-сальниковой связки к основанию лоскута создает опасность травматизации богато васкуляризованных рыхлых структур.
В.Н. Егиев [45] считает целесообразным использование лоскута большого сальника на правой желудочно-сальниковой артерии в случае выполнения реконструкции правой молочной железы (рис. 2, 4). В тех случаях, когда длина сформированного лоскута оказывалась недостаточной для последующего его выведения из брюшной полости, производилась дополнительная мобилизация желудочно-ободочной связки у верхнего края поперечно-ободочной кишки слева направо. Таким образом формировался лоскут большого сальника на сосудистой ножке, представленный правой желудочно-сальниковой артерией и веной.

Рис. 2. Направление мобилизации большого сальника на правой сосудистой ножке.

Рис. 4. Этапы лапароскопической мобилизации лоскута большого сальника на правой сосудистой ножке: а – приподнято тело желудка;
б– клипирование коротких желудочных артерий; в – мобилизация кишечного края большого сальника; г – клипирование левой желудочно-сальниковой артерии; д – рассечение брюшины; е – перемещение лоскута сальника из брюшной полости в область молочной железы (лоскут фиксируется пальцами хирурга).
При заболевании левой молочной железы формируется лоскут большого сальника на питающей сосудистой ножке, состоящей из левой желудочно-сальниковой артерии и вены (рис. 5). В.Н. Егиев подчеркивает, что при таком варианте формирования лоскута возникает необходимость диссекции и разделения нижних коротких артерий желудка. Без выполнения этих манипуляций в зоне желудочно-селезеночной связки лоскут оказывался слишком коротким.

Рис. 5. Схема мобилизации лоскутабольшого сальника на левой сосудистой ножке.
Весь ход операции коррекции молочной железы после органосохраняющей операции можно условно разделить на три этапа: формирование лоскута большого сальника на сосудистой ножке; лапароскопическую миотомию брюшной стенки и эндоскопическое формирование подкожного тоннеля (рис. 6); перемещение сальникового лоскута из брюшной полости к месту реконструкции молочной железы (рис. 7), фиксация лоскута большого сальника и формирование окончательного вида молочной железы (рис. 9).
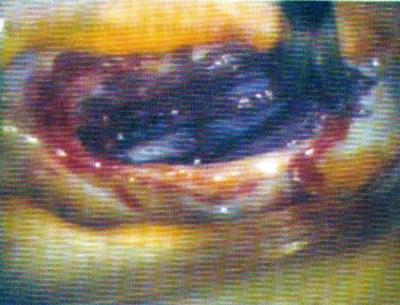
Рис. 6. Формирование подкожного туннеля для перемещения сальникового лоскута
из брюшной полости к мягкотканному дефекту на грудной стенке.

Рис. 7. Этапы формирования подкожного туннеля: а – введение ретрактора; б – расширение оптической полости.
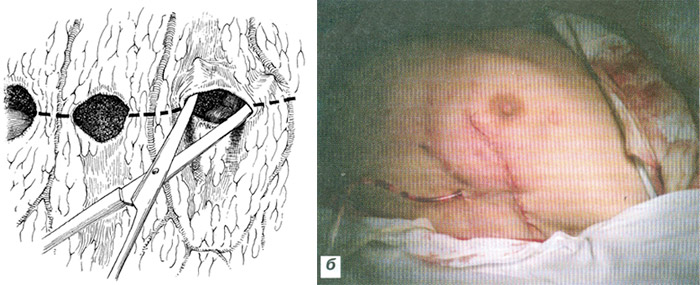
Рис. 9. Замещение дефекта молочной железы лоскутом большого сальника: а – молочная железа с лоскутом большого сальника;
б – окончательный вид после замещения дефекта.
Наиболее важными моментами при эндоскопическом формировании лоскутов большого сальника являются обеспечение надежного гемостаза, оценка состояния сосудов большого сальника, а также интраоперационное обращение с сальником.
Гемостаз является очень важным фактором. Развитие интраоперацинного кровотечения может создать значительные трудности для хирурга и потребовать перехода на лапаротомию. Поэтому рассечение сальника должно производиться по возможности в бессосудитых зонах (рис. 3).

Рис. 3. Рассечение сальника в бессосудистых зонах.
Когда нет уверенности в аваскулярности данного участка, рассечение следует производить при помощи электрокоагуляции (только вдали от магистральных сосудов). Каждые пересекаемый во время операции сосуд должен клипироваться с двух сторон. Следует избегать чрезмерного натяжения ткани сальника во избежание повреждения мелких сосудов, кровотечение из которых может быть не замечено во время операции, но может привести впоследствии к развитию внутрисальниковой гематомы. При формировании сосудистой ножки особую осторожность следует соблюдать на этапе обработки стволов желудочно-сальниковых артерий и вен. Это связано с близким расположением крупных сосудов, обеспечивающих кровоснабжение желудка, двенадцатиперстной кишки, поджелудочной железы и селезенки.
Состояние сосудов большого сальника также очень важно для успешного выполнения реконструкции. Так как сальник представляет собой хорошо васкуляризованную соединительнотканную пластинку, любое угнетение кровообращения вызовет развитие фиброза перемещенного лоскута, существенно снижающего его пластическую ценность. Это тем более важно, что строение сосудистой системы большого сальника отличается чрезвычайной вариабельностью, а формирование лоскута должно производиться с учетом расположения сосудов в каждом конкретном случае [46, 47].
При выполнении любых операций, связанных с использованием большого сальника в качестве пластического материала или применением его для реконструктивно-восстановительных целей, должны соблюдаться определенные правила интраоперационного обращения с формируемым лоскутом.
Оперативное вмешательство следует производить таким образом, чтобы оставлять сальник максимально интактным. Ткань сальника и его мезотелиальный покров чувствителен к воздействию факторов внешней среды – температуры, влажности, а также к механической травматизации. Высушивание, охлаждение, хирургические манипуляции, прикосновение крючков, салфеток, рук хирурга провоцируют в сальнике воспалительные реакции. Эндоскопический доступ предоставляет большие возможности в предупреждении этих последствий. В ходе операции сальник находится в замкнутой брюшной полости, а затем в подкожной клетчатке. Для удержания сальника используют только зажимы с атравматической насечкой – прочие контакты инородных предметов с его тканью исключены.
Особой аккуратности требует перемещение сформированного лоскута из брюшной полости. Здесь необходимо избегать его повреждения о троакары и не применять больших усилий при тракции [42].
Для перемещения сформированного лоскута большого сальника из брюшной полости к дефекту на брюшной стенке необходимо выполнить лапароскопическое рассечение брюшины, внутренней и наружной косых мышц живота латеральнее наружного края влагалища прямой мышцы живота. Рассечение и разведение мышц производится параллельно ходу мышечных волокон каждой из мышц. Таким образом, выполняется косопеременный разрез мышц изнутри, протяженность которого составляет 7-8 см [45].
С помощью аутотрансплантата из лоскута большого сальника объемом 200 см3 становится возможной реконструкция молочной железы не более 2 размера по чашечкам бюстгальтера (рис. 8, 10). Вопрос о реконструкции молочной железы комбинацией собственных тканей (лоскут большого сальника на питающей сосудистой ножке) и силиконового эндопротеза нуждается в более подробной разработке.

Рис. 8. Лоскут большого сальника выведен на грудную стенку для замещения пострезекционного дефекта.
Однако при реконструкции молочной железы лоскутом большого сальника не следует забывать и о последствиях его удаления для брюшной полости. Большой сальник выполняет немаловажную барьерную функцию, т.к. через его сосуды осуществляется миграция гуморальных факторов и клеточных элементов в брюшную полость, он содержит большое количество лимфатических узлов. При воспалении, прободении (язвы, разрывы и т.д.) большой сальник может прирастать к поврежденным органам, ограничивая их от здоровых. В случае внезапных катастроф в брюшной полости большой сальник берет на себя ферментативный «удар», способствуя рассасыванию некротических очагов и рубцеванию. За счет жировой ткани он участвует в терморегуляции, предохраняя внутренние органы от охлаждения.
Особого внимания заслуживает жизнеспособность перемещенного лоскута. На гистологическом уровне показано, что в перемещенном лоскуте большого сальника увеличиваются в размерах адипоциты жировой клетчатки, а также повышается плотность капиллярной сети за счет возрастания vascular endothelial growth factor (VEGF) и стимуляции ангиогенеза. Исследование было выполнено на основании клинических наблюдений небольшого увеличения объема перемещенного лоскута большого сальника, происходившего спонтанно в позднем послеоперационном периоде. В группе из 8 пациентов, которым была выполнена реконструкция молочной железы, были взяты образцы тканей перемещенного сальника во время операции и в позднем послеоперационном периоде. Рост адипоцитов и капиллярной сети перемещенного лоскута еще раз говорит об уникальных регенераторных свойствах большого сальника [47, 48].
Таким образом, активное развитие новых технологий, внедрение эндоскопии практически во все разделы хирургии позволяет по-другому оценить возможности использования сальника в реконструктивных операциях. Разработанные оперативные приемы и модифицированный эндохирургический инструментарий для органосохраняющих и реконструктивно-пластических операций при раке молочной железы дают возможность снизить уровень хирургической агрессии и травматичности вмешательства при сохранении принципов абластики. Пациентки, которые перенесли калечащую операцию радикального удаления молочной железы, в большей степени подвержены депрессиям, и не каждая решается на дополнительное реконструктивное вмешательство.
Использование разработанных эндохирургических методик при выполнении одномоментной реконструкции позволяет избежать или свести к минимуму размеры послеоперационного рубца в донорской зоне, снизить травматичность вмешательства, обусловливая более легкое течение послеоперационного периода, сокращение сроков пребывания в стационаре и временной нетрудоспособности. Легкая мобилизация, прекрасная пластичность и хорошее кровоснабжение обеспечивают реальную перспективу использования большого сальника для восполнения объема молочной железы после различных вариантов подкожной мастэктомии. Однако при выборе данного хирургического метода необходимо соотносить травматичность оперативного вмешательства и возможные осложнения в связи с удалением небезразличного для брюшной полости органа.
Литература
- Morrow M, et al. Correlates of breast reconstruction: results from a population-based study. Cancer. 2005; 104(11): 2340-2346.
- Petersson M, Lundeberg T, Sohlstrom A, Wiberg U, Uvnas-Moberg K. Oxytocin increases the survival of musculocutaneous flaps. Naunyn-Schmiedebergs Arch Pharm. 1998; 357(6): 701-704.
- Боровиков А.М., Желтова Е.В. Эстетические результаты ТРАМ-пластики в отдалённом периоде после мастэктомии. Международный симпозиум пластических хирургов и онкологов. Одесса. 2000; 62-65.
- Блохин С.Н. Первичные реконструктивно-пластические операции в комплексном лечении больных раком молочной железы: Автореф. дис. канд. мед. наук. М., 1996; 23.
- Блохин С.Н., Портной С.М., Лактионов К.П. Реконструкция молочной железы при злокачественных опухолях. Международный симпозиум пластических хирургов и онкологов. Одесса. 2000; 67-75.
- Залуцкий И.В., Шаловая Е.В. Маммопластика у онкологических больных. Анналы пластической, реконструктивной и эстетической хирургии. 2002; 4: 49-50.
- Вишневский А.А., Татьянченко В.К., Алиев Т.Р., Овсянников А.В., Пржедецкий Ю.В., Полякова Н.Б., Шабаршин С.А. Способ пластики молочной железы. №2115369, 1998.
- Friedman R, Argenty LC, Anderson R. Deep inferior epigastric free flap for breast reconstruction afteer radical mastectomy. Plast Reconstr Surg. 1985; 76: 455-458.
- Вишневский А.А. и др. Кожно-жировой лоскут на прямой мышце живота в реконструктивно-восстановительной хирургии молочной железы. Хирургия. 1988; 4: 61-64.
- Аско-Селъяваара С., Смиттен К. Каким способом реконструировать грудь желающим этого? Анналы пластической реконструктивной и эстетической хирургии. 1997; 3: 42-51.
- Чиссов В.И., Трахтенберг А.Х. Атлас онкологических операций. М.: 2008: 5-7.
- Либерманн-Мефферт Д., Уайт X. Большой сальник. Анатомия, физиология, патология, хирургия, исторический очерк. New York: Springer-Verlag. 1989: 336.
- Hultman CS, Carlson GW, Losken A. et al. Utility of the omentum in the reconstruction of complex extraperitoneal wounds and defects: donor-site complications in 135 patients from 1975 to 2000. Ann Surg. 2002; 235: 782-795.
- Das SK. The size of the human omentum and methods of lengthening it for transplantation. Br J Past Surg. 1976; 29: 170-174.
- Емельянов С.И., Матвеев Н.Л., Панченков Д.Н. Лапароскопическое формирование лоскутов большого сальника для целей реконструктивно-восстановительной хирургии. Эндоскопическая хирургия. 2000; 3: 34.
- Емельянов С.И., Матвеев Н.Л., Карташева А.Ф. Эндоскопическое выделение лоскута большого сальника на питающей ножке для замещения пострезекционного дефекта при органосохраняющем лечении рака молочной железы. Эндоскопическая хирургия. 2001; 3: 41.
- Матвеев Н.Л., Панченков Д.Н. Эндовидеохирургические технологии в реконструктивно-восстановительной и пластической хирургии. Эндоскопическая хирургия. 2006; 3: 32-42.
- Hidalgo DA, Saldana EF, Rusch VW. Free flap chest wall reconstruction for recurrent breast cancer and radiation ulcers. Ann Plast Surg. 1993; 30(4): 375-380.
- Kiricuta I. L’utilisation du grand epiploon dans le traitement des fistules post-radio-therapeutiques vesico-vaginales, recto-vesico-vaginales et dans les cysto-plasties. J Chir. 1965; 89: 477-480.
- Kiricuta I. The use great omenlum in the surgery of breast cancer. Presse Med. 1963; 71(1): 15-17.
- Abbes М, Caruso F, Bourgeon Y. Subcutaneous mastectomy. A review of 130 cases. Jut Surg. 1988; 73(2): 107-111.
- Harii K. Microvascular free tissue transfers. World J Surg. 1979; 3: 2933.
- Harii K, Ohmori K, Torn S, Murakami F, Kasai Y, Sekiguchi J, Ohmori S. Free groin skin flap. Br J Plast Surg 1975; 28: 225-258.
- Fissette J. Le Lambeau epiploque dows la reconstruction mammaire. Acta Chir Belg. 1980; 79: 115.
- Irons GВ, Arnold PG. Use of the omenial free flap for soft-tissue reconstruction. Ann Plast Surg. 1983; 11(6): 501-507.
- Jurkiewicz MJ, Arnold PG. The omentum: An account of its use in the reconstruction of the chest wall. Ann Surg. 1977; 185(5): 548-551.
- Lee АВ, Schimbert G, Shatkin S. Total excision of the aternum and thoracic pedicle transposition of the greater omentum: useful strategies in managing severe mediastinal infection following open heart surgery. Surgery. 1976; 80(4): 433-436.
- Goldwyn RM. Aesthetic concepts of reconstruction after radical mastectomy. St. Louis: С.V. Mosby. 1978; 267.
- Hidalgo DA, Disa JJ, Cordeiro PG, Hu QY. A review of 716 consecutive free flaps for oncologic surgical defects: refinement in donor-site selection and technique. Plast Reconstr Surg. 1998; 102(3): 722-732.
- Contant CME, van Geel AN, van der Holt B, Wiggers T. The pedicled omentoplasty and split skin graft for reconstruction of large chest wall defects: A validity study of 34 patients. Eur J Surg Oncol. 1996; 22: 532.
- Paige КТ, Bostwick J, Bried JТ, Jones G. A comparison of morbidity from bilateral, unipedicled and unilateral, unipedicled TRAM flap breast reconstructions. Plast Reconstr Surg1998; 101(7): 1819-1827.
- Романов В.А. Эндоскопический атлас. 2-е изд. М.: 2001: 220.
- Shilov BL. Great omentum autotransplantation in plastic surgery. Plast Reconstr Surg. 2004; 114: 1342.
- Yamashita K, Shimizu K. Endoscopic video-assisted breast surgery: procedures and short-term results. J Nihon Med Sch. 2006; 73(4): 193-202.
- Saltz R, Stowers R, Smith M, Gadacz TR. Laparoscopically harvested omental free flap to cover a large soft tissue defect. Ann Surg. 1993; 217(5): 542-547.
- Bostwick J, Hill HL, Nahai F. Repairs in the lower abdomen, groin or perineum with myocutaneous or omental flaps. Plast Reconstr Surg. 1979; 63: 186-189.
- Barrow OL, Nahai F, Tindall GT. The use of greater omentum vascularized free flaps for neurosurgical disorders requiring reconstruction. J Neurosurg. 1984; 60(2): 305-311.
- Bostwick J, et al. Endoscopic plastic surgery. St Louis: Quality Medical. 1995; 287.
- Cothier-Savey I, Tamtawi В, et al. Immediate breast reconstruction using a laparoscopically harvested omental flap. Plast Reconstr Surg. 2001; 107(5): 1156-1163, discussion 1164-1165.
- Эндоскопические методики в хирургии молочной железы. Эндоскопическая хирургия 2005; 1/2: 196-197.
- Zaha H, Onomura M, Nomura H, Umekawa K, Oki M. Free omental flap for partial breast reconstruction after breast-conserving surgery. Plast Reconstr Surg. 2012; 129(3): 583-587.
- Zaha H, Inamine S, Naito T, Nomura H. Laparoscopically harvested omental flap for immediate breast reconstruction. Am J Surg. 2006; 192(4): 556-558.
- Zaha H, Sunagawa H, Kawakami K, Touyama T, Yonaha T, Ohshiro N. Partial breast reconstruction for an inferomedial breast carcinoma using an omental flap. World J Surg. 2010; 34(8): 1782-1787.
- Емельянов С.И., Матвеев Н.Л., Панченков Д.Н., Черноземов П.В., Владыкин А.Л., Карташева А.Ф. Лапароскопический способ формирования лоскута большого сальника на сосудистой ножке. Гос. рег. №2000106106, 15.03.2000.
- Егиев В.Н. Хирургия малых пространств. М.: 2008; 88-98.
- Миланов Н.О., Сандриков В.А., Шилов Б.Л., Буторин А.Г. Гемодинамические особенности микрохирургической аутотрансплантации большого сальника. Вестник хирургии. 1990; 144(1): 90-92.
- Costa SS, Blotta RM, Mariano MB, Meurer L, Edelweiss MI. Laparoscopic treatment of Poland’s syndrome using the omentum flap technique. Clinics (Sao Paulo). 2010; 65(4): 401-406.
- Costa SS, Blotta RM, Meurer L, Edelweiss MI. Adipocyte morphometric evaluation and angiogenesis in the omentum transposed to the breast: a preliminary study. Clinics (Sao Paulo). 2011; 66(2): 307-312.

