Результаты органосохраняющих операций с интраоперационной электронной и дистанционной гамма-терапией у больных раком молочной железы T1-2No-1Mo
Мусабаева Л.И., Лисин В.А., Слонимская Е.М., Дорошенко А.В.
Научно-исследовательский институт онкологии Сибирского отделения РАМН, Томск, Россия
Опубликовано: Журнал «Онкохирургия», 2012, том 4, №2.
Изучена эффективность органосохраняющих операций, сочетающихся с интраоперационной и дистанционной лучевой терапией, у больных раком молочной железы T1-2No-1Mo.
Приведены данные пятилетнего наблюдения 370 больных раком молочной железы РМЖ T1-2No-1Mo, из которых 252 пациентки составляли исследовательскую группу, а 118 больных – контрольную. Пациенткам исследовательской группы выполнена органосохраняющая операция, во время которой проведена интраоперационная лучевая терапия электронным пучком с энергией 6 МэВ в дозе 10 Гр. В дальнейшем этой же группе проведена дистанционная гамма-терапия в стандартном режиме фракционирования. Суммарная курсовая доза интраоперационной и дистанционной лучевой терапии с учетом временного интервала между этими процедурами составила 60 изоГр. Больным контрольной группы после органосохраняющей операции на оставшуюся молочную железу проводили только дистанционную гамма-терапию в суммарной дозе 50 Гр. Сроки наблюдения – от 1 года до 5 лет. У больных с применением смешанной лучевой терапии и в контрольной группе изучали частоту возникновения местных рецидивов, показатели безрецидивной, метастатической и общей выживаемости.
За пятилетний период рецидивы рака молочной железы в основной группе были диагностированы у 6 (2,38%) больных, а в контрольной группе – у 13 (11%) больных (р=0,001). В первой группе, по сравнению с контрольной, достигнуты достоверно значимые результаты: уменьшение частоты местных рецидивов, увеличение показателей безрецидивной и общей выживаемости.
Таким образом, метод лечения больных раком молочной железы, включающий органосохраняющую операцию, интраоперационную и дистанционную лучевую терапию, обеспечивает более высокую эффективность лечения по сравнению с методом, в который интраоперационная терапия не включена.
Ключевые слова: рак молочной железы, органосохраняющая операция, интраоперационная электронная и дистанционная гамма-терапия, пятилетнее наблюдение.
Введение
В настоящее время интраоперационную лучевую терапию (ИОЛТ) проводят в онкологических центрах на всех континентах, и один раз в два года проходят международные симпозиумы по этой проблеме. Число больных раком молочной железы (РМЖ), которые перенесли органосохраняющее лечение с ИОЛТ или ИОЛТ и дистанционной гамма-терапией (ДГТ) в различных клиниках стран Европы и Америки, достигает уже несколько тысяч. В 1998 году было образовано международное общество по применению ИОЛТ (ISIORT). В октябре 2010 года в Аризоне (США) состоялся очередной конгресс Международного общества ИОЛТ, на котором были представлены результаты комбинированного лечения с ИОЛТ злокачественных новообразований различных локализаций из институтов и радиологических центров Европы, Америки и России, в т.ч. Москвы, Томска и Обнинска [1]. К обсуждаемым вопросам, касающимся назначения ИОЛТ или смешанной лучевой терапии (ИОЛТ и ДГТ), относится оценка эффективности нового метода лечения у больных РМЖ после проведения органосохраняющей операции (ОСО). До настоящего времени единой точки зрения в отношении выбора однократной дозы ИОЛТ, эффективности метода лечения, характера осложнений, возможности сочетания с ДГТ нет. Поэтому исследования, как считают многие ученые за рубежом и в России, следует продолжать, т.к. сохраняется перспектива применения данного метода. Оценку эффективности комбинированного лечения после ОСО с ИОЛТ и ДГТ у больных РМЖ T1-2No-1Mo проводят с учетом пятилетних результатов. В НИИ онкологии СО РАМН г. Томск смешанную лучевую терапию с ИОЛТ и ДГТ при раке молочной железы T1-2No-1Mo применяют с 2005 года, и опубликованы материалы, касающиеся различных аспектов применения нового метода [2-4].
Цель работы – изучить эффективность органосохраняющих операций, сочетающихся с интраоперационной и дистанционной лучевой терапией, у больных РМЖ T1-2No-1Mo.
Материалы и методы
Под наблюдением находились 370 больных РМЖ T1-2No-1Mo, которые распределялись на две группы – исследовательскую (252 больные) и контрольную (118 пациенток). Всем больным на первом этапе выполняли ОСО. В первой группе операции сопровождались проведением ИОЛТ в однократной дозе 10 Гр на «ложе» удаленной опухоли с последующим выполнением ДГТ на всю оставшуюся молочную железу. ИОЛТ проводили пучком быстрых моноэнергетических электронов с энергией 6 МэВ на бетатроне МИБ-6Э, который расположен непосредственно в операционной. Больным контрольной группы после ОСО на оставшуюся молочную железу проводили только ДГТ в суммарной дозе 50 Гр на гамма-аппарате THERATRON.
ДГТ в основной группе проводили в стандартном режиме фракционирования так, чтобы суммарная курсовая доза ИОЛТ и ДГТ с учетом временного интервала между этими процедурами составила 60 изоГр. Длительность временного интервала между ИОЛТ и ДГТ не была постоянной, а изменялась в зависимости от состояния пациентки после перенесенной операции. Поэтому для нахождения числа сеансов послеоперационной гамма-терапии было получено математическое выражение, учитывающее длительность временного интервала между ИОЛТ и ДГТ. Это выражение имеет вид:
![]()
где ВДФпр – предельно допустимое значение фактора Время – Доза – Фракционирование;
ΔTп – временной интервал в сутках между ИОЛТ и ДЛТ;
dф и Δtф – соответственно однократная доза и временной интервал для выбранного фракционированного режима облучения.
При наиболее часто встречающемся значении фактора ВДФпр = 100 ед. выражение будет иметь вид:
![]()
При проведении ИОЛТ и ДГТ осуществлялось необходимое дозиметрическое планирование, при котором в обеих группах были рассчитаны пространственные распределения дозы в облучаемом объеме тела. В основной группе рассчитано также суммарное распределение поглощенной дозы, создаваемое электронами при ИОЛТ и гамма-излучением при ДГТ.
На рисунке 1 приведен общий вид гистограммы дозного поля в относительных единицах, образованного только гамма-излучением при гамма-терапии с двух встречных полей (А), а также показано суммарное распределение дозы электронов и гамма-излучения (Б). При сравнении гистограмм А и Б отчетливо видно локальное увеличение поглощенной дозы на гистограмме Б, создаваемое электронным пучком при ИОЛТ непосредственно в зоне «ложа» удаленной опухоли.
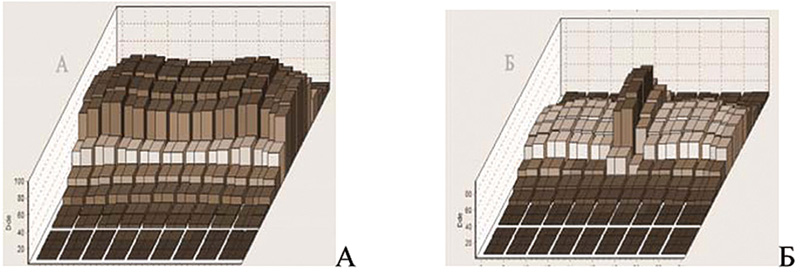
Рисунок 1. Характер пространственного распределения дозы гамма-излучения (А)
и суммарной дозы электронов и гамма-излучения (Б) в относительных единицах.
Сроки наблюдения за больными составляли от 1 года до 5 лет. В обеих группах оценивали частоту рецидивов, показатели безрецидивной, метастатической и общей выживаемости. Продолжительность жизни больных без признаков рецидива и общую выживаемость высчитывали моментным методом по Kaplan-Meier c применением log-rank-теста. Для статистической обработки данных использовали программу Statistica 6.0.
Результаты исследования и обсуждение
За пятилетний период наблюдения рецидивы РМЖ T1-2No-1Mo были диагностированы у 6 (2,38 %) больных, которые получили ИОЛТ и ДГТ, и у 13 (11%) – в контрольной группе. При использовании смешанной лучевой терапии (ИОЛТ и ДГТ) рецидивы опухоли наблюдали достоверно реже, чем после применении только ДГТ в контрольной группе (р=0,001) (табл. 1).
Таблица 1. Частота и сроки появления местных рецидивов опухоли.
| Сроки наблюдения, годы |
Число больных, абс. (%) | |
|---|---|---|
| Группа I ИОЛТ+ДГТ, n=252 |
Группа II ДГТ, n=118 |
|
| 1 | 1 (0,39) | 3 (2,5) |
| 2 | 3 (1,19) | 4 (3,4) |
| 3 | 2 (0,79) | 2 (1,7) |
| 4 | 0 | 1 (0,8) |
| 5 | 0 | 3 (2,5) |
| Всего | 6 (2,38)* | 13 (11) |
Примечание: * различия статистически значимы по сравнению с контрольной группой (р<0,05).
При изучении частоты и сроков возникновения местных рецидивов установлено, что в группе больных, получавших ИОЛТ и ДГТ, практически все рецидивы были выявлены в течение первых 3 лет наблюдения. Из них в зоне проведения ИОЛТ рецидивы опухоли возникли только у 3 больных (1,19%), тогда как в группе контроля рецидивы практически равномерно возникали на протяжении всего 5-летнего периода наблюдения. У больных контрольной группы рецидивы за пятилетний период наблюдения отмечены у 13 (11%).
Показатели 5-летней безрецидивной выживаемости в исследуемой группе оказались достоверно выше, составив 97,3±1,08%, тогда как у больных контрольной группы – 86,7±3,5% (р=0,02) (табл. 2, рис. 2).
Таблица 2. Показатели безрецидивной выживаемости.
| Сроки наблюдения, годы |
Безрецидивная выживаемость, % | |
|---|---|---|
| Группа I ИОЛТ+ДГТ, n=252 |
Группа II ДГТ, n=118 |
|
| 1 | 99,6±0,3 | 97,4±1,4 |
| 2 | 98,7±0,7 | 94±2,1 |
| 3 | 97,3±1,08 | 92,2±2,4 |
| 4 | 97,3±1,08 | 91,2±2,6 |
| 5 | 97,3±1,08* | 86,7±3,5 |
| р=0,02 | ||
Примечание: * различия статистически значимы в сравнении с контрольной группой (р<0,05).
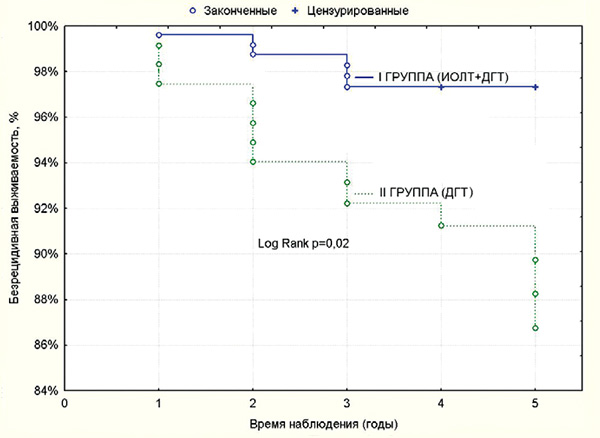
Рисунок 2. Безрецидивная выживаемость больных РМЖ T1-2No-1Mo
в зависимости от применяемого метода лучевой терапии.
Развитие гематогенных метастазов у больных, которым проводили ИОЛТ и ДГТ, выявлено за пятилетний период наблюдения у 14 (5,56%) больных. Более высокая частота развития отдаленных метастазов наблюдалась в контрольной группе с ДГТ – у 16 больных (13,5%,), что было значимо больше, чем в основной исследуемой группе (р=0,01). При этом показатели 5-летней безметастатической выживаемости (табл. 3, рис. 3) в исследуемой группе имели тенденцию повышения показателей относительно группы контроля и составили 92,2±2,1% и 86,3±3,1% соответственно (р>0,05).
Таблица 3. Частота и сроки появления метастазов у больных исследуемых групп.
| Сроки наблюдения, годы |
Количество больных, абс. (%) | |
|---|---|---|
| Группа I ИОЛТ+ДГТ, n=252 |
Группа II ДГТ, n=118 |
|
| 1 | 3 (1,19) | 3 (2,5) |
| 2 | 8 (3,17) | 2 (1,7) |
| 3 | 3 (1,19) | 4 (3,4) |
| 4 | 0 | 3 (2,5) |
| 5 | 0 | 4 (3,4) |
| Всего | 14 (5,56)* | 16 (13,5) |
Примечание: * различия статистически значимы по сравнению с контрольной группой (р<0,05).
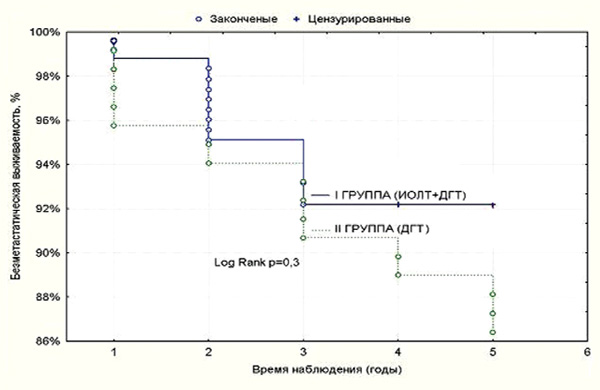
Рисунок 3. Безметастатическая выживаемость больных РМЖ
в зависимости от метода лучевой терапии.
От прогрессирования основного заболевания за пятилетний период наблюдения погибли 5 (2,4%) пациенток, получивших смешанную лучевую терапию (ИОЛТ и ДГТ), и 12 (10,1%) больных, которым проводили ДГТ в стандартном режиме. Как следует из данных, летальные исходы достоверно чаще наблюдались у пациенток, получавших только ДГТ (р<0,05).
Аналогичная закономерность выявлена и в отношении показателей общей 5-летней выживаемости, которые составили 97,8±0,9% и 89,7±2,7% соответственно (р=0,03) (табл. 4, рис. 4).
Таблица 4. Показатели общей выживаемости в зависимости от метода лучевой терапии.
| Сроки наблюдения, годы |
Общая выживаемость, % | |
|---|---|---|
| Группа I ИОЛТ+ДГТ, n=252 |
Группа II ДГТ, n=118 |
|
| 1 | 99,5±0,4 | 98,3±1,1 |
| 2 | 98,3±0,8 | 97,4±1,4 |
| 3 | 97,8±0,9 | 94±2,1 |
| 4 | 97,8±0,9 | 92,3±2,4 |
| 5 | 97,8±0,9 | 89,7±2,7* |
| р=0,03 | ||
Примечание: * различия статистически значимы по сравнению с I группой (р<0,05).
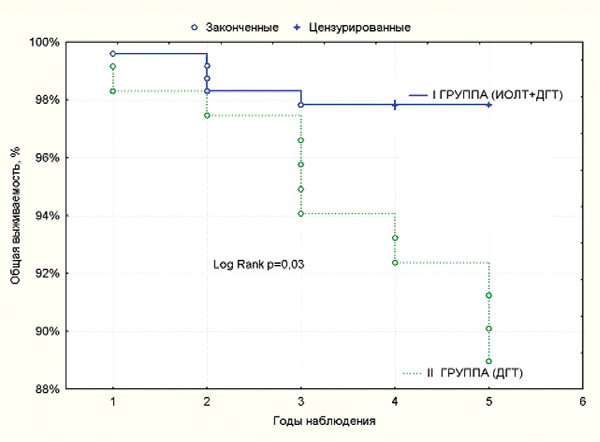
Рисунок 4. Общая выживаемость больных РМЖ T1-2No-1Mo после органосохраняющей операции
в зависимости от применяемого метода лучевой терапии.
Заключение
Проведенные исследования показали, что рецидивы опухоли РМЖ после ОСО и смешанной лучевой терапии (ИОЛТ+ДГТ) наблюдались значимо реже, чем после применения адъювантной ДГТ в стандартном режиме у больных контрольной группы (р=0,001), что расценивается отдельными авторами как появление роста новых очагов РМЖ. Нельзя исключить и возможность возникновения у отдельных больных рецидивов рака в молочной железе вследствие мультицентричного характера роста опухоли, который не был выявлен на этапах диагностики.
Полученные данные свидетельствуют также о том, что метод лечения, включающий ИОЛТ на «ложе» удаленной опухоли в однократной дозе 10 Гр, позволяет достоверно уменьшить частоту возникновения местных рецидивов РМЖ T1-2No-1Mo, увеличить показатели безрецидивной выживаемости в сравнении с пациентками, которые в послеоперационном периоде получали только ДГТ в суммарной очаговой дозе 50 Гр. Кроме того, у больных РМЖ T1-2No-1Mo после ОСО, дополненной проведением ИОЛТ и ДГТ, произошло достоверное снижение частоты летальных исходов и соответственно увеличение показателей 5-летней общей выживаемости по сравнению с больными контрольной группы.
Литература
- Медведев Ф.В., Мардынский Ю.С., Гулидов И.А., Смирнова И.А. Интраоперационная лучевая терапия рака молочной железы. Онкохирургия 2010; 2(3): 46-51.
- Мусабаева Л.И., Жогина Ж.А., Лисин В.А, Слонимская Е.М., Дорошенко А.В. Интраоперационная электронная и дистанционная гамма-терапия в органосохраняющем лечении больных раком молочной железы. Медицинская радиология и радиационная безопасность 2010; 55(5): 42-47.
- Слонимская Е.М., Мусабаева Л.И., Дорошенко А.В. и др. Коллиматор для облучения мягких тканей и молочной железы. Патент на полезную модель № 71074 от 27 февраля 2008.
- Новая медицинская технология ФС №2010/386 «Комплексное лечение больных раком молочной железы с применением интраоперационной электронной и дистанционной гамма-терапии при органосохраняющих операциях» от 26 октября 2010.

